Enhavo forigita Enhavo aldonita
Kiel registrite je 20:26, 24 sep. 2018
Kalia sulfido
Dosiero:Potassium sulfide.png
Plata kemia strukturo de la Kalia sulfido
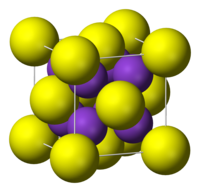
Kristala strukturo de la Kalia sulfido
Alternativa(j) nomo(j)
Kemia formulo K2 S
CAS-numero-kodo 1312-73-8
ChemSpider kodo 142491
PubChem-kodo 162263
Fizikaj proprecoj
Aspekto senkoloraj aŭ flavecaj kristaloj
Molara maso 110257 g·mol-1
Denseco 1,74g cm−3
Fandpunkto 840 °C
Bolpunkto 912 °C
Mortiga dozo (LD50) 400 mg/kg (buŝe)
Sekurecaj Indikoj
Riskoj R17 R23 [[Listo da R-
Deklaroj#R25|R25]] R31 R34 R50
Sekureco S24 S26 [[Listo da S-
Deklaroj#R45|S45]]
Pridanĝeraj indikoj
Danĝero
GHS Damaĝo Piktogramo
GHS Signalvorto Damaĝa
GHS Deklaroj pri damaĝoj H251 , H300 , H314 , H318 , H371
GHS Deklaroj pri antaŭgardoj P235+410 , P260 , P264 , P270 , P280 , P301+310 , P301+330+331 , P303+361+353 , P304+340 , P305+351+338 , P309+311 , P310 , P321 , P330 , P363 , P405 , P407 , P413 , P420 , P501
Escepte kiam indikitaj, datumoj estas prezentataj laŭ iliaj
normaj kondiĉoj pri temperaturo kaj premo
Kalia sulfido aŭ K2 S estas neorganika kombinaĵo, senkolora solidaĵo rare trovata pro ĝia forta reakciemo kun akvo. Ĝi estas la baza substanco de vasta familio de polisulfidoj tiaj kiaj kalia du-, tri-, kvar- kaj kvin-sulfidoj. Ĝi uzatas kiel fungicido, baktericido kaj insekticido en agrikulturo kaj kiel kemia reakcianto en laboratorio. En akva solvaĵo ĝi produktas iomete bazan reakcion. Kalia sulfido estiĝas kiam nigra pulvo brulas kaj ĝi estas grava peranto en multaj piroteknikaj efikoj.
Sintezoj Reakcioj
Reakcio 1 kalia sulfido reakcias kun acidoj:
N
a
2
S
+
2
H
C
l
⟶
2
N
a
C
l
+
H
2
S
{\displaystyle {\mathsf {Na_{2}S+2\;HCl\longrightarrow 2NaCl+H_{2}S}}}
Reakcio 2 Fortaj acidoj atakas kalian sulfidon:
N
a
2
S
+
3
H
2
S
O
4
⟶
S
O
2
+
S
+
2
H
2
O
+
2
N
a
H
S
O
4
{\displaystyle {\mathsf {Na_{2}S+3H_{2}SO_{4}\longrightarrow SO_{2}+S+2\;H_{2}O+2\;NaHSO_{4}}}}
Reakcio 3
3
N
a
2
S
+
2
K
M
n
O
4
+
4
H
2
O
⟶
2
M
n
O
2
+
6
N
a
O
H
+
2
K
O
H
+
3
S
{\displaystyle {\mathsf {3\;Na_{2}S+2\;KMnO_{4}+4\;H_{2}O\longrightarrow 2\;MnO_{2}+6\;NaOH+2\;KOH+3\;S}}}
Reakcio 4 Per hejtado kun jodo kalia sulfido estas reduktata:
N
a
2
S
+
I
2
=
2
N
a
I
+
S
{\displaystyle {\mathsf {Na_{2}S+I_{2}=2\;NaI+S}}}
Reakcio 5
N
a
2
S
+
4
K
O
C
l
⟶
K
2
S
O
4
+
4
K
C
l
{\displaystyle {\mathsf {Na_{2}S+4\;KOCl\longrightarrow K_{2}SO_{4}+4\;KCl}}}
Reakcio 6
K
2
S
+
2
O
2
⟶
K
2
S
2
O
3
+
2
K
O
H
{\displaystyle {\mathsf {K_{2}S+2\;O_{2}\longrightarrow K_{2}S_{2}O_{3}+2\;KOH}}}
Literaturo Referencoj