Kobalta (III) hidroksido
kemia kombinaĵo
| Kobaltika hidroksido | |||||
| Kemia formulo | |||||
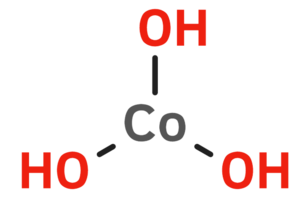 | |||||
Kobalta (III) hidroksido | |||||
 | |||||
| Alternativa(j) nomo(j) | |||||
| |||||
| CAS-numero-kodo | 1307-86-4 | ||||
| ChemSpider kodo | 8278661 | ||||
| PubChem-kodo | 14785 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | malhelverda aŭ bruna solidaĵo[1][2] | ||||
| Molmaso | 109,954g mol−1 | ||||
| Denseco | 4,46 g/cm−3 | ||||
| Fandpunkto | 100°C | ||||
| Acideco (pKa) | 15,7 [3] | ||||
| Kps | Akvo:1,6 x 10-44 [4] | ||||
| Mortiga dozo (LD50) | 550 mg/kg (buŝe) | ||||
| GHS etikedigo de kemiaĵoj | |||||
| GHS Damaĝo Piktogramo |
| ||||
| GHS Signalvorto | Damaĝa substanco | ||||
| GHS Deklaroj pri damaĝoj | H302, H317, H319, H330, H334, H360, H372 | ||||
| GHS Deklaroj pri antaŭgardoj | P201, P202, P260, P261, P264, P270, P271, P272, P280, P281, P284, P301+312, P302+352, P304+340, P304+341, P305+351+338, P308+313, P310, P314, P320, P321, P330, P333+313, P337+313, P342+311, P363, P403+233, P405, P501 | ||||
(25 °C kaj 100 kPa) | |||||
Kobalta (III) hidroksido aŭ trihidroksido de kobalto estas neorganika kombinaĵo apartenanta al la familio de la hidroksidoj, rezultanta el hidratagado de la kobalta oksido aŭ hidrolizo de kobaltaj saloj. Kobalta (III) hidroksido estas malhelverda aŭ bruna solidaĵo, nesolvebla en akvo. Kobalta (III) hidroksido prezentas tri hidroksilajn grupojn ligitajn al kobaltatomo. Ĝi konsistas je 1 kobaltatomo, 3 hidrogenatomoj, 3 oksigenatomoj kaj uzatas en kemiaj sintezoj. Ekzistas 4 kondiĉoj por la kobaltaj hidroksidoj, nome, du kobaltaj (II) hidroksidoj estas rozkoloraj kaj bluaj, kaj du kobaltaj (III) hidroksidoj estas verdaj aŭ brun-koloraj.
Reakcioj
redaktiReakcio 1
redakti- Preparado de kobalta (III) hidroksido per traktado de kobalta (III) oksido kun akvo:
Reakcio 2
redakti- Reakcio de kobalta (III) sulfato kun baria hidroksido donante kobaltan (III) hidroksidon:
Reakcio 3
redakti- Preparado de kobalta (III) hidroksido per hidrolizo de la kobalta (II) klorido:
Reakcio 4
redakti- Preparado de kobalta (III) oksido per senhidratigado de kobalta (III) hidroksido:
Reakcio 5
redakti- Reakcio de kobalta (III) hidroksido kun klorida acido donante kobaltan (III) kloridon:



