Oktanalo
kemia kombinaĵo
| Oktanalo | ||||
 | ||||
| Plata kemia strukturo de la Oktanalo | ||||
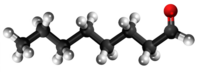 | ||||
| Tridimensia kemia strukturo de la Oktanalo | ||||
| Alternativa(j) nomo(j) | ||||
| ||||
| Kemia formulo | ||||
| CAS-numero-kodo | 124-13-0 | |||
| ChemSpider kodo | 441 | |||
| PubChem-kodo | 454 | |||
| Fizikaj proprecoj | ||||
| Aspekto | senkolora likvaĵo kun penetranta odoro je frukto | |||
| Molmaso | 128,2120 g·mol-1 | |||
| Denseco | 0,822g cm−3[1] | |||
| Fandpunkto | 12°C-15°C[2] | |||
| Bolpunkto | 163,4°C[3] | |||
| Refrakta indico | 1,4217 | |||
| Ekflama temperaturo | 51,7 °C[4] | |||
| Solvebleco | Akvo:0,21 g/L | |||
| Sekurecaj Indikoj | ||||
| Riskoj | R10 | |||
| Sekureco | S16 | |||
| Pridanĝeraj indikoj | ||||
| Danĝero
| ||||
| GHS Damaĝo Piktogramo |
| |||
| GHS Signalvorto | Averto | |||
| GHS Deklaroj pri damaĝoj | H226, H315, H319, H411, H412 | |||
| GHS Deklaroj pri antaŭgardoj | P210, P233, P240, P241, P242, P243, P264, P273, P280, P302+352, P303+361+353, P305+351+338, P321, P332+313, P337+313, P362, P370+378, P391, P403+235, P501[5] | |||
(25 °C kaj 100 kPa) | ||||
Oktanalo aŭ C8H16O estas kemia kunmetaĵo, senkolora likvaĵo kun penetranta odoro je frukto apartenanta al la funkcia grupo de la aldehidoj. Ĝi estas nesolvebla en akvo kaj komerce uzata en la fabrikado de parfumoj kaj kiel gustigagento. Ĝi ordinare estas produktata per hidroformiligo de la hepteno aŭ senhidrogenigo de la oktanolo. Oktanalo estas brulema substanco kaj neakordigebla kun fortaj oksidigagentoj, fortaj reduktigagentoj kaj fortaj bazoj.
Sintezoj
redaktiSintezo 1
redakti- Preparado per reduktigo de la oktanata acido:
Sintezo 2
redakti- Preparado ekde la oktanolo:
Sintezo 3
redakti- Preparado ekde la oktilamino:
Sintezo 4
redakti- Preparado ekde la oktanamido:
Sintezo 5
redakti- Preparado ekde la heptano:
Sintezo 6
redakti- Preparado ekde la heksano:
Sintezo 7
redakti- Preparado ekde la oktila klorido:
Reakcioj
redaktiReakcio 1
redakti- Konvertado al oktanata acido:
Reakcio 2
redakti- Konvertado al oktanolo:
Reakcio 3
redakti- Konvertado al oktilamino en acida medio:
Reakcio 4
redakti- Konvertado al oktanamido:
Reakcio 5
redakti- Konvertado al heptano:
Reakcio 6
redakti- Sapigo de la Oktanalo:
Reakcio 7
redakti- Reakcio kun HCl:




