Izoamila sulfido
| Izoamila sulfido | ||
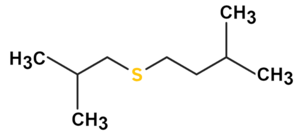 | ||
| Plata kemia strukturo de la Izoamila sulfido | ||
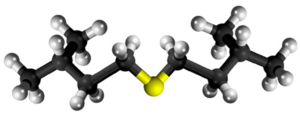 | ||
| Tridimensia kemia strukturo de la Izoamila sulfido | ||
| Alternativa(j) nomo(j) | ||
| ||
| Kemia formulo | ||
| CAS-numero-kodo | 544-02-5 | |
| ChemSpider kodo | 10525 | |
| PubChem-kodo | 10990 | |
| Fizikaj proprecoj | ||
| Aspekto | flava, brulema, rapidbola kaj toksa likvaĵo kun penetranta odoro | |
| Molmaso | 174,347 g·mol−1 | |
| Denseco | 0,834g cm−3[1] | |
| Fandpunkto | -74,6 °C[2] | |
| Bolpunkto | 212,8 °C[3] | |
| Refrakta indico | 1,453 | |
| Ekflama temperaturo | 76,4 °C[4] | |
| Solvebleco | Akvo:Malmulte solvebla | |
| Sekurecaj Indikoj | ||
| Riskoj | R36/37/38 | |
| Sekureco | S26 S36/37/39 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Damaĝa substanco | |
| GHS Deklaroj pri damaĝoj | H315, H319 | |
| GHS Deklaroj pri antaŭgardoj | P264, P280, P302+352, P305+351+338, P321, P332+313, P337+313, P362 | |
(25 °C kaj 100 kPa) | ||
Izoamila sulfido aŭ C10H22S estas kemia kombinaĵo, apartenanta al la funkcia grupo de la esteroj de la sulfida acido kaj izoamila alkoholo. Izoamila sulfido estas flava, brulema, rapidbola kaj toksa likvaĵo kun penetranta odoro, analiza reakciaĵo uzata en kemiaj sintezoj kaj en la fabrikado de kosmetikaĵoj kaj farmaciaĵoj. Kutime ĝi estiĝas per kondensiĝa reakcio aŭ per esterigo de Fischer-Speyer kun sulfata acido kiel katalizilo. Izoamila sulfido estas malmulte solvebla en akvo, sed tute solvebla en alkoholo, duetila etero, kloroformo kaj plejmulto el la organikaj solvantoj. Izoamila sulfido reakcias kun fortaj oksidigagentoj kaj fortaj bazoj. Sulfidaj esteroj malkomponiĝas per varmigo aŭ kun la tempopaso en sulfuro aŭ sulfuraj derivaĵoj.
Sintezoj
redaktiSintezo 1
redakti- Preparado per agado de sulfida acido kaj izoamila alkoholo:
Sintezo 2
redakti- Preparado per traktado de natria sulfido kaj izoamila alkoholo:
Sintezo 3
redakti- Preparado per reakcio de sulfida acido kaj izoamila klorido:
Sintezo 4
redakti- Preparado per interagado de natria sulfido kaj izoamila klorido:[5]
Sintezo 5
redakti- Preparado per interagado de metila sulfido kaj izoamila formiato:
Sintezo 6
redakti- Preparado per acida transesterigo inter sulfida acido kaj izoamila benzoato:
Sintezo 7
redakti- Preparado per traktado de duizoamil-sulfuroksido kaj jodida acido:
Reakcioj
redaktiReakcio 1
redakti- Hidrolizo de la izoamila sulfido:
Reakcio 2
redakti- Sapigo de la izoamila sulfido:
|
+2 natria sulfido+2 |
Reakcio 3
redakti- Reakcio per acida transesterigo kun formiata acido:
Reakcio 4
redakti- Reakcio per alkohola transesterigo kun metila alkoholo:
Reakcio 5
redakti- Reakcio per acida transesterigo kun benzoata acido:
Reakcio 6
redakti- Reakcio kun NH3:
Reakcio 7
redakti- Reakcio kun HCl:
Literaturo
redakti- Molbase
- Warmed-Over Flavor of Meat
- Reprint and Circular Series of the National Research Council
- Toxic substances control act
- Chemistry of organic sulfur compounds in petroleum and petroleum products
- Chemistry and technology of synthetic liquid fuels
- Thermophysical properties research literature retrieval guide
- Soviet Electrochemistry


