Kalia stanato
kemia kombinaĵo
| Kalia stanato (IV) | |||
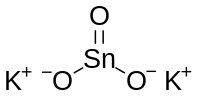 | |||
| Plata kemia strukturo de la Kalia meta-stanato (IV) K2SnO3 | |||
 | |||
| Plata kemia strukturo de la Kalia orto-stanato (VI) K2SnO4 | |||
 | |||
| Tridimensia kemia strukturo de la Kalia meta-stanato (IV) | |||
| Kompleksa formulaĵo de Kalia meta-stanato.3 H2O | |||
| Alternativa(j) nomo(j) | |||
| |||
| Kemia formulo | .3 H2O | ||
| CAS-numero-kodo | 12027-61-1 (anhidra) | ||
| CAS-numero-kodo | (trihidatigita) 12142–33–5 (trihidatigita) | ||
| PubChem-kodo | 61554 | ||
| Merck Index | 15,7791 | ||
| Fizikaj proprecoj | |||
| Aspekto | senkolora aŭ blanka solidaĵo | ||
| Molmaso | 244904 g·mol−1 | ||
| Denseco | 3,197g cm−3[1] | ||
| Fandpunkto | 140 °C (malkomponiĝas) | ||
| Solvebleco | Akvo:reakcias | ||
| Mortiga dozo (LD50) | 178 mg/kg (buŝe)[2] | ||
| Sekurecaj Indikoj | |||
| Riskoj | R34 R36/37/38 | ||
| Sekureco | S26 S36/37/39 S45 | ||
| Pridanĝeraj indikoj | |||
| Danĝero
| |||
| GHS Damaĝo Piktogramo |
| ||
| GHS Signalvorto | Averto | ||
| GHS Deklaroj pri damaĝoj | H315, H319, H335 | ||
| GHS Deklaroj pri antaŭgardoj | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P403+233, P405, P501[3] | ||
(25 °C kaj 100 kPa) | |||
Kalia stanato (IV) aŭ K2SnO3.3 H2O estas neorganika kombinaĵo de kalio, stano kaj oksigeno, senkolora aŭ blanka substanco kun orto-romba kristala strukturo, dum ĝia analogo K4SnO4 estas triklina[4]. Stanatoj troviĝas sub du formoj: metastanatoj prezentantaj la jonon SO3−2 kaj ortostanatoj (IV) aŭ SO4−2.
Sintezoj
redaktiSintezo 1
redakti- Preparado de stanato de kalio per traktado de stana (IV) oksido kaj kalia hidroksido[5]:
|
|
Sintezo 2
redakti- Varmigo de orto-stanato de kalio konvertas ĝin sinsekve al K2SnO3, K2Sn3O7 kaj SnO2[6]:
- Malkomponado 1
|
|
- Malkomponado 2
|
|
- Malkomponado 3
|
|
Sintezo 2
redakti- Stanito de kalio reakcias kun bismuta hidroksido por doni kalian stanaton:
|
|
Sintezo 3
redakti- Preparado ekde tri-stanato de kalio kaj kalia hidroksido:
|
|
Reakcioj
redaktiReakcio 1
redakti- Stanato (IV) de kalio reakcias kun akvo:
|
|
Reakcio 2
redakti- Stanato (IV) de kalio reakcias kun fortaj acidoj:
|
|
Reakcio 3
redakti- Stanato de kalio reakcias kun tiostanato de kalio kaj klorida acido:
|
|
Reakcio 4
redakti- Stanato de kalio reakcias kun halogenidoj por doni heksa-stanatojn:
|
|
Reakcio 5
redakti- Stanato de kalio reakcias kun karbona duoksido:
|
|
Reakcio 6
redakti- Stanato de kalio reakcias kun kalcia nitrato:
|
|


