Akrilata acido
kemia kombinaĵo
| 2-Propenata acido | |||||

| |||||
| Plata kemia strukturo de la Akrilata acido | |||||
| |||||
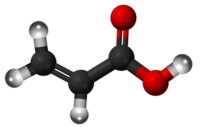
| Tridimensia strukturo de la Akrilata acido | |||||
| Alternativa(j) nomo(j) | |||||
| |||||
| Kemia formulo | |||||
| CAS-numero-kodo | 79-10-7 | ||||
| ChemSpider kodo | 6333 | ||||
| PubChem-kodo | 6581 | ||||
| Merck Index | 15,121 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | senkolora kaj travidebla likvaĵo kun akre acida odoro | ||||
| Molmaso | 72.0627 g·mol-1 | ||||
| Denseco | 1.051 g cm−3 | ||||
| Fandpunkto | 14 °C | ||||
| Bolpunkto | 141 °C | ||||
| Refrakta indico | 1,4224 | ||||
| Ekflama temperaturo | 68 °C | ||||
| Memsparka temperaturo | 429 °C | ||||
| Solvebleco | Akvo: | ||||
| Mortiga dozo (LD50) | 2590 mg/kg (buŝe) | ||||
| Sekurecaj Indikoj | |||||
| Risko | R10 R20/21/22 R35 R50 | ||||
| Sekureco | S26 S36/37/39 S45 S61 | ||||
| Pridanĝeraj indikoj | |||||
| Danĝero
| |||||
| GHS etikedigo de kemiaĵoj | |||||
| GHS Damaĝo-piktogramo |
| ||||
| GHS Signalvorto | Damaĝa substanco | ||||
| GHS Deklaroj pri damaĝoj | H226, H332, H312, H302, H314, H335, H400 | ||||
| GHS Deklaroj pri antaŭgardoj | P210, P261, P273, P303+361+353, P304+340, P310, P305+351+338 | ||||
Akrilata acido estas organika kombinaĵo, plej simpla nesaturita karboksilata acido, konsistante je unu vinila grupo (C=C-) rekte ligita al la radikalo karboksila. Ĝi estas senkolora likvaĵo kun akre acida odoro, kaj miksiĝas kun akvo, alkoholoj, eteroj kaj kloroformo.
Pli ol milionoj da tunoj estas ĉiujare produktitaj. Biologie, kelkaj specioj de algoj ankaŭ produktas akrilatan acidon. Testoj faritaj en ratoj elmontras ke la akrilata acido estas embriotoksa kaj teratogenagento, tamen, ĝi ne estas klasita kiel homa karcinomogenera. Toksiĝoj povas okazi per inhlado, ingestado aŭ kontakto kun okuloj kaj haŭto.
Sintezoj
redaktiSintezo 1
redakti- Depende de la kondiĉoj, propileno povas estigi akroleinon, akrilatan acidon aŭ acetono:
- Preparado de akroleino per interagado de propileno kun oksigeno:
Sintezo 2
redakti- Per interagado de la acetileno kun karbona unuoksido en akva medio:
Sintezo 3
redakti- Per aldona reakcio inter la keteno kaj la formaldehido:
- Preparado de akrilata acido per interagado de keteno kun formaldehido:
Sintezo 4
redakti- Kvankam ne komerca, la interagado de la acetata acido kun la formaldehido ankaŭ estas interesa metodo por produktado de akrilata acido:[1]
- Preparado de akrilata acido per interagado de acetata acido kun formaldehido:
Sintezo 5
redakti- Acetileno reakcias kun nikel-karbonilo, klorida acido kaj akvo por estigi akrilatan acidon:
Literaturo
redakti- NIST Chemistry WebBook
- Toxipedia Arkivigite je 2017-03-29 per la retarkivo Wayback Machine
- Chemical Book
- Australian Government
- Chemicalland21
- Catalysis in Petrochemical Processes, M.S. Matar, M.J. Mirbach, H.A. Tayim
Kunrilataj kemiaĵoj
redaktiVidu ankaŭ
redaktiReferencoj
redakti- ↑ Industrial Organic Chemicals, Harold A. Wittcoff, Bryan G. Reuben, Jeffery S. Plotkin







