Apiino
| Apiino | ||
 | ||
| Plata kemia strukturo de la Apiino | ||
 | ||
| Tridimensia kemia strukturo de la Apiino | ||
 | ||
| Apiino estas flava antioksidigaĵo trovata en plantoj tia kia la Apium graveolens[1] | ||
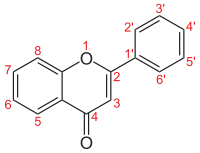 | ||
| Numerigo de la karbonaj strukturoj de la flavonoj. | ||
| Kemia formulo | ||
| CAS-numero-kodo | 26544-34-3 | |
| ChemSpider kodo | 4444321 | |
| PubChem-kodo | 5280746 | |
| Merck Index | 15,719 | |
| Fizikaj proprecoj | ||
| Aspekto | flava solidaĵo | |
| Molmaso | 564,496 g·mol-1 | |
| Denseco | 1,74g cm−3 | |
| Fandpunkto | 230°C[2] | |
| Bolpunkto | 942,2°C[3] | |
| Refrakta indico | 1,744 | |
| Ekflama temperaturo | 316,7 °C | |
| Acideco (pKa) | 6,11 | |
| Solvebleco | Akvo:1,53 g/L [4] | |
| Mortiga dozo (LD50) | 4837 mg/kg (buŝe) | |
| Sekurecaj Indikoj | ||
| Riskoj | R36/37/38 | |
| Sekureco | S26 S36 | |
| Pridanĝeraj indikoj | ||
| Danĝero
| ||
| GHS Damaĝo Piktogramo |
| |
| GHS Signalvorto | Averto | |
| GHS Deklaroj pri damaĝoj | H315, H319, H335 | |
| GHS Deklaroj pri antaŭgardoj | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P321, P332+313, P337+313, P362, P403+233, P405, P501[5] | |
(25 °C kaj 100 kPa) | ||
Apiino aŭ C26H28O14 estas natura kombinaĵo vaste distribuita en la planto-regno, apartenanta al la familio de la flavonoidoj, flava amargusta solidaĵo kun antiinflamigaj, antivirusaj, antimalariaj, antireproduktivaj kaj antioksidigaj proprecoj. Ĝi estas grande trovata en herboj kaj plantoj tiaj kiaj Apium graveolens, Lemna minor kaj Petroselinum sativum.
Grandkvante ĝi povas esti hepatotoksa, insekticida, vazodilatiga kaj emenagoga. Apiino estas nesolvebla en akvo, alkoholo kaj duetila etero, sed solvebla en varma akvo, varma alkoholo kaj alkalaj solvaĵoj. Dioskorido kaj Plinio la Maljuna uzis la petroselon kaj parolis pri iliaj medicinaj uzoj.[6] Apiinaj infuzaĵoj, kvankam ili plibonigas nian imunan sistemon, ili povas esti abortigaj kaj toksaj kiam grandvante. En la fino de la 18-a jarcento, Stanislaus von Kostanecki esploris multajn flavonoidoj inklude de la apiino.
Sintezoj
redaktiSintezo 1
redakti- Preparado ekde la apigenino:
Sintezo 2
redakti- Preparado ekde la kempferolo per forigo de hidroksila grupo en la 3-a pozicio de la kromenonila grupo:
Sintezo 3
redakti- Preparado ekde la krizino per aldono de hidroksila grupo en la 4-a pozicio de la fenila grupo:
Sintezo 4
redakti- Preparado ekde la kverketino per aldono de du hidroksilaj grupoj, unu en la 3-a pozicio de la kromenonila ringo kaj alia en la 5-a pozicio de la fenila ringo:
Sintezo 5
redakti- Preparado ekde la luteolino per forigo de hidroksila grupo en la 5-a pozicio de la fenila grupo:
Sintezo 6
redakti- Preparado ekde la miriketino per forigo de tri hidroksilaj grupoj, unu en la 3-a pozicio de la kromenonila ringo kaj du hidroksilaj grupoj en la 3-a kaj 5-a pozicioj de la fenila ringo:
Sintezo 7
redakti- Preparado ekde la naringenino per oksidado en la 2-a pozicio de la kromenonila grupo:
Sintezo 8
redakti- Konvertado al fisetino per forigo de du hidroksilaj grupoj, unu en la 3-a pozicio de la kromenonila grupo kaj alia en la 3-a pozicio de la fenila grupo:
Reakcioj
redaktiReakcio 1
redakti- Konvertado al apigenino aldono de 2 akvo-molekuloj:
Reakcio 2
redakti- Konvertado al kempferolo per aldono de hidroksila grupo en la 3-a pozicio de la kromenonila grupo:
Reakcio 3
redakti- Konvertado al krizino per forigo de hidroksila grupo en la 4-a pozicio de la fenila grupo:
Reakcio 4
redakti- Konvertado al kverketino per aldono de du hidroksilaj grupoj, unu en la 3-a pozicio de la kromenonila ringo kaj alia en la 5-a pozicio de la fenila ringo:
Reakcio 5
redakti- Konvertado al luteolino per aldono de hidroksila grupo en la 5-a pozicio de la fenila grupo:
Reakcio 6
redakti- Konvertado al miriketino per aldono de tri hidroksilaj grupoj, unu en la 3-a pozicio de la kromenonila ringo kaj du hidroksilaj grupoj en la 3-a kaj 5-a pozicioj de la fenila ringo:
Reakcio 7
redakti- Konvertado al naringenino per reduktado en la 2-a pozicio de la kromenonila grupo:
Reakcio 8
redakti- Konvertado al "fisetino" per aldono de du hidroksilaj grupoj, unu en la 3-a pozicio de la kromenonila grupo kaj alia en la 3-a pozicio de la fenila grupo:
Literaturo
redakti- Science Direct
- Advances in Carbohydrate Chemistry and Biochemistry
- Handbook of Biotransformations of Aromatic Compounds
- Enzyme Handbook
- Chemfaces
- NCBI Resources
- Herbal Medicines in Pregnancy and Lactation: An Evidence-Based Approach
- Dictionary of Food Compounds with CD-ROM: Additives, Flavors, and Ingredients


