Sukcenata acido
| Sukcenata acido | ||
| ||

| ||

| ||
| Alternativa(j) Nomo(j) | ||
| Butanodiojka acido etano-1,2-dukarboksilata acido E363 | ||
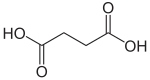
| Kemia formulo | C4H6O4 aŭ HOOC-(CH2)2-COOH | |
| PubChem-kodo | 1110 | |
| ChemSpider kodo | 1078 | |
| CAS-numero-kodo | 110-15-6 | |
| Karakterizaĵoj | ||
| Acideco (pKa) | pka1= 4.16 pKa2 = 5.61 | |
| Molmaso | 118.09 g·mol-1 | |
| Smiles | C(CC(=O)O)C(=O)O | |
| Denseco | 1.56 g/cm3 (20 °C) | |
| Memsparka temperaturo |
630 °C | |
| Fandopunkto | 184 °C (363 ℉; 457 K) | |
| Bolpunkto | 235 °C (455 ℉; 508 K) | |
| Akva solvebleco | 58g/L (20 °C) | |
| Ekflama temperaturo | 206 °C (403 ℉; 479 K) | |
| Sekurecaj Indikoj | ||
| Riskoj | R36 | |
| Sekureco | S26 | |
| Pridanĝeraj indikoj | ||
| Pridanĝeraj indikoj | ||
| Danĝero |
| |
Sukcenata acido[1] aŭ butanodiojka acido kaj historie konata kiel spirito de sukceno estas duprotona, dukarboksilata acido kun kemia formulo C4H6O4 kaj struktura formulo HOOC-(CH2)2-COOH. Ĝi estas blanka kaj senodora solidaĵo. La sukcinato plenumas gravan rolon en la ciklo de citrata acido, energi-produktanta procezo. La nomo derivas el la latina succinum, kiu signifas sukceno[2], el kiu la acido estas produktebla.
Produktado kaj reakcio
redaktiLa spirito de sukceno originale estis estigita el la sukceno pere de pulvorigado kaj distilado tra iu sablobano.
La sukcenata acido produktiĝas per pluraj manieroj. La ordinara industria metodologio inkludas hidrogenigon de maleata acido, oksidadode 1,4-butanoduolo kaj karboniligo de la etilena glikolo[3]. Pli juŝe, la sukcenata acido estas produktata per fermentado de glukozo ekde renovigeblaj krudmaterialoj kaj plipurigado de la krude biologibaza sukcenata acido[4].
La sukcenata acido estas konvertebla al fumarata acido pere de oksidado[5]. La duetila estero restas kiel substrato en la kondensiĝo de Stobbe[6]. La malhidratigo de la sukcenata acido estigas sukcenatan anhidridon[7].
Uzoj
redaktiLa sukcenata acido estas antaŭanto al kelkaj specifaj poliesteroj[8]. Ĝi same estas komponanto en kelkaj alkidaj rezinoj[9]. La sukcenata acido uzatas en la nutraĵo- kaj trinkaĵo- industrio, ĉefe kiel acidokontrolilo. La entute monda produktado taksatas je 16 mil al 30 mil tunoj/jare, kaj kun jara kresko je 10%. La kresko estas atribuebla al la avancoj de la industria bioteknologio, kiu penas substitui la kemiaĵojn surbaze de petrolo en la industriaj aplikadoj. Kelkaj industrioj tiel kiel BioAmber, Reverdia, Myriant, BASF kaj Purac progresas en la industriskala produktado de sukcenata acido biologibaza al komercodisponebleco.
Ĝi ankaŭ vendatas kiel nutroaldonaĵo kaj pordieta suplementaro[10], kaj ĝenerale ĝi estas konsiderata sekura por uzado de la Usona Administracio por Manĝo kaj Drogo. Kiel aldonilo[11] en la farmaciaj produktoj ĝi uzatas por kontroli la acidecon, kaj malpli ofte, en eferveskaj piloloj[12][13].
Biokemio
redaktiLa sukcenato estas peranto en la ciklo de la citrata acido kaj kapablas doni elektronojn al la elektronotransporta ĉeno (ETC) per la reakcio:
Ĉi-konvertiĝo katalizatas de la enzimo sukcenata malhidrogenazo[15] (aŭ la komplekso II de la mitokondria ETC[16]). La komplekso estas iu lipoproteino ligita al 4-subunua membrano kiu promocias la oksidadon de la sukcenato al la reduktado de la ubikinono[17]. La perantaj elektronaj transportiloj estas la FAD[18] kaj tri grupoj de 2Fe-2S kiel parto de la subunuo B[19].
Sukcenata acido same estiĝas kiel flankprodukto en la fermentado de sukero. Ĝi pruntedonas al la fermentitaj drinkaĵoj tiel kiel vino kaj biero ian ordinaran guston kiu estas kombinaĵo de saleco, amareco kaj acideco.
La saloj de la sukcenata acido estas nomataj sukcenatoj. Unu ekzemplo estas la natria sukcenato[20], iu blanka, akvosolvebla salo. La esteroj de la sukcenata acido ankaŭ estas nomataj sukcenatoj: unu ekzemplo estas la dumetila sukcenato, kies molekula formulo estas (CH2CO2CH3)2[21].
La sukcenata acido estas grava peranta biokemiaĵo okazanta en ĉiuj vivestuloj. Same kiel la aliaj unu- kaj du- karboksilataj acidoj, ĝi ne estas konsiderita danĝera, kvankam ĝi estas iritohaŭta. La sukcenatoleo estas produktata per varmigo de la sukcenata acido.
Kombinaĵoj
redaktiVidu ankaŭ
redaktiReferencoj
redakti- ↑ A System of Chemistry for the Use of Students of Medicine, Franklin Bache
- ↑ Life in Amber, George O. Poinar
- ↑ Renewable Polymers: Synthesis, Processing, and Technology, Vikas Mittal
- ↑ Eco-Architecture V: Harmonisation between Architecture and Nature, C.A. Brebbia, R. Pulselli
- ↑ Handbook of Food Toxicology, S.S. Deshpande
- ↑ Organic Reactions: Mechanism With Problems, Rajpal Tyagi
- ↑ Food Additive Toxicology, Maga
- ↑ Plastics from Bacteria: Natural Functions and Applications, George Guo-Qiang Chen
- ↑ La alkidaj rezinoj estas produkteblaj laŭ reakcio inter unu acido, unu alkoholo kaj unu sekiga oleo.
- ↑ CRC Handbook of Food Additives, Second Edition, Volume 1, Thomas E. Furia
- ↑ Excipient Development for Pharmaceutical, Biotechnology, and Drug Delivery ..., Ashok Katdare, Mahesh Chaubal
- ↑ Eferveskaj piloloj estas kuraciloj por kontrolo de stomakacideco.
- ↑ Pharmaceutical Salts and Co-crystals, Johan Wouters, David E. Thurston
- ↑ Protein: The Basis of All Life, J. E. R. McDonagh
- ↑ Bioprocessing for Value-Added Products from Renewable Resources: New ..., Shang-Tian Yang
- ↑ An Introduction to Agricultural Biochemistry, J.M. Chesworth, T. Stuchbury, J.R. Scaife
- ↑ Krause's Food & the Nutrition Care Process, L. Kathleen Mahan, Janice L Raymond, Sylvia Escott-Stump
- ↑ FAD: flavina adenina nukleotido.
- ↑ Molecular Mechanisms in Bioenergetics, L. Ernster
- ↑ PubChem
- ↑ The Lipid Handbook, Second Edition, Frank D. Gunstone, John L. Harwood, Fred B. Padley
